Coronavirus EE. UU.: ¿Por qué se ha detenido el ensayo pediátrico de Astrazeneca?
La Universidad de Oxford ha detenido las pruebas en niños y adolescentes de la vacuna que desarrolla con AstraZeneca. Aquí todos los detalles.
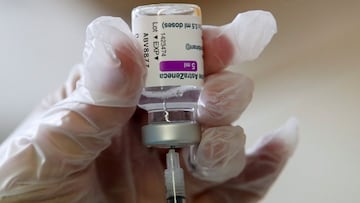
Por varios meses, algunos gobiernos de Europa se han cuestionado sobre la producción, suministros y efectos secundarios de la vacuna de AstraZeneca. Incluso, varios países han suspendido temporalmente el uso de esta vacuna contra el coronavirus, ya que surgieron informes sobre sus posibles efectos secundarios.
Mientras las investigaciones al respecto continúan, la Universidad de Oxford ha decidido detener el ensayo pediátrico de la vacuna que desarrolla con AstraZeneca.
Coronavirus EE. UU.: ¿Por qué se ha detenido el ensayo pediátrico de AstraZeneca?
La Universidad de Oxford informó que suspenderá el ensayo pediátrico de la vacuna de AstraZeneca hasta que la Agencia Reguladora de Medicamentos del Reino Unido (MHRA por sus siglas en inglés) proporcione más información sobre su investigación de casos raros de trombosis.
El ensayo pediátrico de la vacuna de AstraZeneca para menores de entre seis y 17 años comenzó en febrero de este año para comprobar si generan una respuesta inmune suficiente contra el coronavirus.
A pesar de que el estudio se encuentra detenido, la Universidad de Oxford recomienda a los participantes asistir a las visitas que tenían programadas. La universidad también comunicó que las pruebas de la vacuna en niños y adolescentes no presentan problemas de seguridad; sin embargo, esperarán las conclusiones de la MHRA.
Agencias reguladoras investigan la vacuna AstraZeneca
La semana pasada, la Agencia Reguladora de Medicamentos del Reino Unido señaló que, hasta finales de marzo, identificaron 30 casos de coágulos de sangre entre los 18,1 millones de personas que recibieron la vacuna de AstraZeneca.
De los 30 incidentes, 22 corresponden a trombosis del seno venoso cerebral (CVST por sus siglas en inglés). Los casos restantes están relacionados con la coagulación de sangre con bajo nivel de plaquetas.
Después de revisar la evidencia, la Agencia Europea del Medicamento (EMA por sus siglas en inglés) concluyó que los coágulos de sangre inusuales deben incluirse como efectos secundarios muy raros de la vacuna de AstraZeneca.
El comité de seguridad de la EMA tomó en consideración todas las pruebas disponibles actualmente, incluido el asesoramiento de un grupo especial de expertos. La EMA enfatiza que los beneficios generales de la vacuna de AstraZeneca para prevenir el coronavirus superan los riesgos de efectos secundarios.
La Organización Mundial de la Salud (OMS) y otros organismos reguladores también están estudiando detenidamente los últimos datos sobre la vacuna de AstraZeneca, en espera de que no haya alguna razón para cambiar la evaluación de esta sobre sus beneficios contra el coronavirus.
- AstraZeneca
- Universidad Oxford
- OMS
- Ciencia
- Industria farmacéutica
- Coronavirus
- Farmacia
- Virología
- Enfermedades infecciosas
- Universidad
- ONU
- Enfermedades
- Microbiología
- Educación superior
- Salud pública
- Medicina
- Empresas
- Sistema educativo
- Política sanitaria
- Organizaciones internacionales
- Economía
- Educación
- Sanidad
- Relaciones exteriores
- Biología
- Industria
- Ciencias naturales
- Salud






